Властивості алюмінію: питома вага і теплопровідність, виробництво, застосування, сплави і температура плавлення
Алюміній — всім відомий з шкільного курсу хімії елемент таблиці Менделєєва. У більшій частині з’єднань він проявляє трехвалентность, але в умовах високих температур досягає деякої міри окислення. Одним з найбільш важливих його сполук є оксид алюмінію.
Основні характеристики алюмінію
Алюміній — сріблястий метал з питомою вагою 2,7*103кг/м3 і густиною 2,7 г/см3. Легкий і пластичний, гарний, як провідник електроенергії, завдяки тому, що теплопровідність алюмінію досить висока — 180 ккал/м*год*град (вказаний коефіцієнт теплопровідності). Теплопровідність алюмінію перевищує аналогічний показник чавуну в п’ять разів і заліза в три рази.
Завдяки своєму складу, цей метал можна легко розкачати в тонкий лист або витягнути в дріт. При зіткненні з повітрям на його поверхні утворюється оксидна плівка (оксид алюмінію), яка є захистом від окислення і забезпечує його високі антикорозійні властивості. Тонкий алюміній, наприклад, фольга або порошок цього металу миттєво згорають, якщо їх нагрівати до високих температур і стають оксидом алюмінію.
Метал не особливо стійкий до агресивних кислот. Приміром, його можна розчинити в сірчаної або соляної кислоти навіть, якщо вони разбавленны, особливо, якщо їх нагрівати. Однак він не розчиняється в розведеною в концентрованої і при цьому холодної азотній кислоті, завдяки оксидній плівці. Певний вплив на метал мають водні розчини лугів — оксидний шар розчиняється і утворюються солі, що містять цей метал в складі аніона — алюмінати.
Відомо, що алюміній є найбільш часто зустрічається металом у природі, але вперше в чистому вигляді його зміг отримати вчений-фізик з Данії Х. Ерстед ще в 1925 році XIX століття. Цей метал займає третє місце за поширеністю в природі елементів і є лідером серед металів. 8,8% алюмінію містить земна кора. Його виявили у складі слюд, польових шпатів, глин і мінералів.
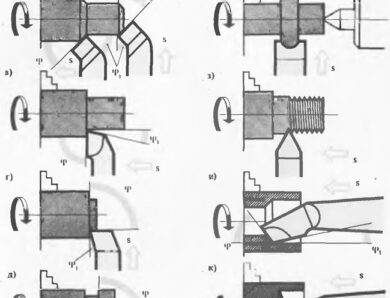
Виробництво і застосування алюмінію
Процес виробництва дуже енергоємний і тому перший великий завод у нашій країні був побудований і запущений в XX столітті. Основною сировиною для отримання цього металу є оксид алюмінію. Щоб його отримати, необхідно мінерали, що містять алюміній або боксити, очистити від домішок. Далі електролітичним способом розплавляють природний або отриманий штучним шляхом кріоліт при температурі трохи нижче 1000 ?С . Потім починають потроху додавати оксид алюмінію і супутні речовини, необхідні для поліпшення якості металу. В процесі оксид починає розкладатися і виділяється алюміній. Чистота одержуваного металу 99,7% і вище.
Цей елемент знайшов своє застосування в харчовому виробництві в якості фольги і столових приладів, у будівництві використовують його сплави з іншими металами, в авіації, електротехніці в якості замінника міді для кабелів, як легирующая добавка в металургії, алюмотермии та інших галузях.
Що таке температура плавки металів?
Температура плавки металів – значення температури нагрівання металу, при якій починається процес переходу з початкового стану в інший, тобто процес протилежний кристалізації (тужавіння), але нерозривно пов’язаний з нею.
Отже, для розплавлення метал нагрівають ззовні до температури плавлення і продовжують нагрівати для подолання межі фазового переходу. Суть в тому, що показник температури плавлення означає температуру, при якій метал знаходиться в фазовому рівновазі, тобто між рідким і твердим тілом. Іншими словами існує одночасно, як в тому, так і в іншому стані. А для плавлення потрібно нагріти його більше прикордонної температури, щоб процес пішов в потрібну сторону.
Варто сказати про те, що тільки для чистих складів температура плавки постійна. Якщо в складі металу знаходяться домішки, то це змістить кордон фазового переходу, а, відповідно, і температура плавлення буде інший. Це пояснюється тим, що склад з домішками має іншу кристалічну структуру, в якій атоми взаємодіють між собою по-іншому. Виходячи з цього принципу, метали можна розділити на:
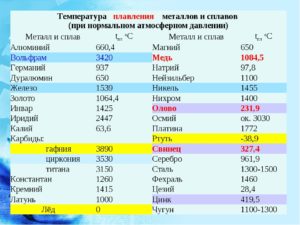
- легкого плавлення, такі як ртуть і галій, наприклад, (температура плавлення до 600°С)
- среднеплавкие — це алюміній і мідь (600-1600°С)
- тугоплавкі — молібден , вольфрам (більше 1600°С).
Знання показника температури плавлення необхідно, як при виробництві сплавів для правильного розрахунку їх параметрів, так і при експлуатації виробів з них, оскільки цей показник визначає обмеження їх використання. Вже давним давно для зручності вчені фізики звели ці дані в одну таблицю. Існують таблиці температур плавки як металів, так і їх сплавів.
Температура плавлення алюмінію
Плавлення — процес перероблення металів зазвичай в спеціальних печах для отримання сплаву потрібної якості в рідкому стані . Як вже говорилося вище, алюміній належить до среднеплавким металів і плавиться при нагріванні до 660?С. При виготовленні виробів з металу температура плавлення впливає на вибір плавильної печі або агрегату і, відповідно, використовуваних для відливання вогнетривких форм.
Зазначена температура відноситься до процесу плавки чистого алюмінію. Так як в чистому вигляді він застосовується рідше, а введення в його склад домішок змінює температуру плавлення. Сплави алюмінію виготовляються для того, щоб змінити які-небудь його властивості, збільшити міцність, жаростійкість. В якості добавок застосовують:
- цинк
- мідь
- магній
- кремній
- марганець.
Додавання домішок тягне за собою зниження електропровідності, погіршення або поліпшення корозійних властивостей, підвищення відносної щільності.
Зазвичай додавання інших елементів у метал призводить до того, що температура плавлення сплаву знижується, але не завжди. Приміром, додавання міді в обсязі 5,7% призводить до зниження температури плавлення до 548?С. Отриманий сплав називають дюралюминием, його піддають подальшій термічній загартуванню. А алюмінієво-магнієві сполуки плавляться при температурі 700 — 750?С.
Під час процесу плавлення необхідний суворий контроль температури розплаву, а також присутності газів в складі, які виявляють через технологічні проби або способом вакуумної екстракції. На заключній стадії виробництва сплавів алюмінію проводять їх модифікування.